- 21412
- 产品价格:面议
- 发货地址:上海金山石化 包装说明:不限
- 产品数量:9999.00 个产品规格:不限
- 信息编号:144789385公司编号:14235332
- 袁小姐 经理 微信 13818104617
- 进入店铺 在线留言 QQ咨询 在线询价
十堰MDRCE认证 专业正规可靠-需要什么材料
- 相关产品:
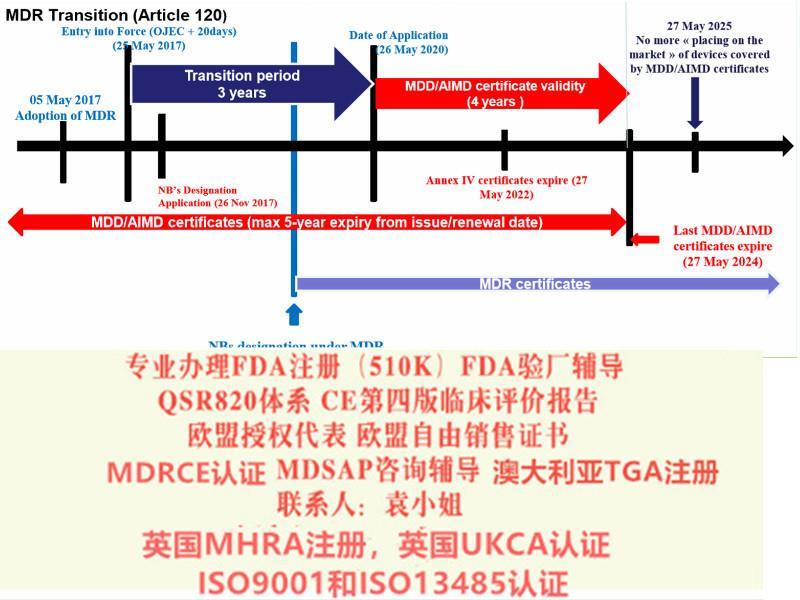
2019年2月医疗器械法规(MDR)和体外诊断医疗器械法规(IVDR)较终提案发布

MDR将有源医疗器械指令(现行的90/385/EEC)纳入了进来

我公司专业办理医疗产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证,全套CE技术文件编订, CE第四版临床评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,医疗器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请), FDA QSR820验厂辅导及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改,英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)。
关于CE新版临床评价报告MEDDEV 2.7.1的编写流程
法规背景
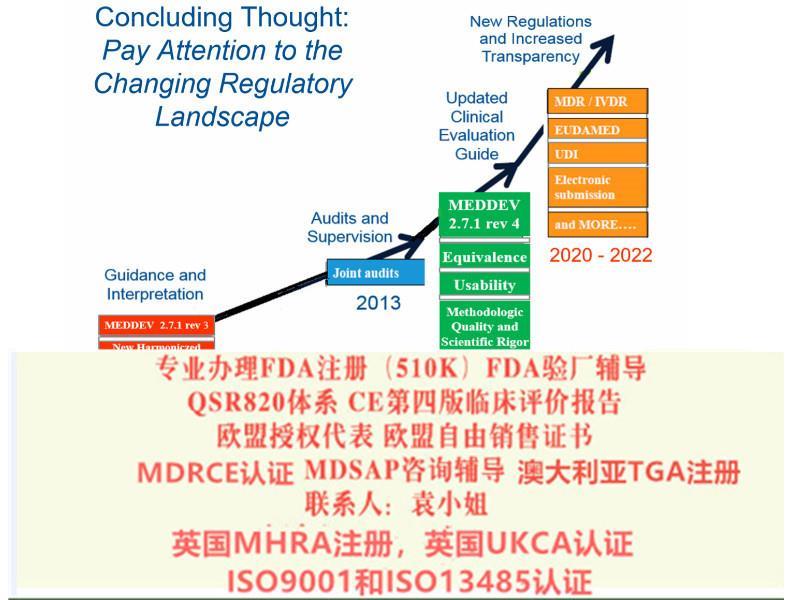
2016年6月,欧盟**(European Commission)发布了第四版医疗器械临床评价的指导原则(MEDDEV 2.7.1 Rev.4)。和2009年第三版的指导原则相比,直观的变化就是文件的页数从46页变为了65页,更新的版本不仅包含了新的要求,还有对以前要求的进一步细化,扩展和澄清,同时还有一些举例以帮助生产商实施临床评价
MEDDEV2.7/1从性质上来说是一份指导原则,所以它没有所谓的“生效日期”,由每一个公告机构自行决定第三版的失效日期及第四版的实施日期。目前大多数的公告机构如TUV南德(NB 0123)已经不再接受基于第三版指导原则的临床评价报告;之前按照第三版完成临床评价获得CE证书的产品也会在监督审核的时候被要求按照第四版进行补充评价即更新撰写。
此外,该指导原则的发布时间碰巧在2016年6月15日MDR(草稿)文本发布之后,所以指导原则的要求也与新法规的临床评价的要求较为接近。所以该指导原则可以作为向新法规过渡的一个工具。
全套CE技术文件编订,医疗器械出口企业在申请CE认证时,不管是I类普通产品还是II/III类高风险产品,都必须要提供第四版临床报告。全套CE技术文件编订已经拿到CE证书的企业,今年监督审核也需要提供。全套CE技术文件编订在TUV,***等公告机构监督审核报告中明确开出不符合项目要求该版本的要求针对于MDD指令和AIMD指令,全套CE技术文件编订,将要申请或者已经拿到了TUV莱茵、TUV南德、***或其他公告机构CE证书的企业,一定要高度关注。
CE技术文件编订
全套CE技术文件编订临床报告的内容:
1、器械的性能测试报告;
2、器械的依据协调标准进行的测试报告;
3、器械PMS数据;
4、器械的PMCF的数据;
5、文献资料中搜集到的器械*和性能的数据;
6、比对器械的数据。
CE技术文件编订
全套CE技术文件编订相对于之前的临床报告,第四版的临床报告主要变化体系在:
1.临床报告更新的频率
2.报告编写人和评价人的资质
3.评估报告需要有明确的可测量目标
4.确定技术发展水平
5.数据的科学性和有效性
6.比对器械
7.比对器械的数据获得
8.什么时候需要临床试验
9.售后监督和售后临床跟踪
10.风险—收益。

至2020年5月26日,MDR法规将*强制实施

MDR将有源医疗器械指令(现行的90/385/EEC)纳入了进来

我公司专业办理医疗产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证,全套CE技术文件编订, CE第四版临床评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,医疗器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请), FDA QSR820验厂辅导及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改,英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)。
关于CE新版临床评价报告MEDDEV 2.7.1的编写流程
法规背景
2016年6月,欧盟**(European Commission)发布了第四版医疗器械临床评价的指导原则(MEDDEV 2.7.1 Rev.4)。和2009年第三版的指导原则相比,直观的变化就是文件的页数从46页变为了65页,更新的版本不仅包含了新的要求,还有对以前要求的进一步细化,扩展和澄清,同时还有一些举例以帮助生产商实施临床评价
MEDDEV2.7/1从性质上来说是一份指导原则,所以它没有所谓的“生效日期”,由每一个公告机构自行决定第三版的失效日期及第四版的实施日期。目前大多数的公告机构如TUV南德(NB 0123)已经不再接受基于第三版指导原则的临床评价报告;之前按照第三版完成临床评价获得CE证书的产品也会在监督审核的时候被要求按照第四版进行补充评价即更新撰写。
此外,该指导原则的发布时间碰巧在2016年6月15日MDR(草稿)文本发布之后,所以指导原则的要求也与新法规的临床评价的要求较为接近。所以该指导原则可以作为向新法规过渡的一个工具。
全套CE技术文件编订,医疗器械出口企业在申请CE认证时,不管是I类普通产品还是II/III类高风险产品,都必须要提供第四版临床报告。全套CE技术文件编订已经拿到CE证书的企业,今年监督审核也需要提供。全套CE技术文件编订在TUV,***等公告机构监督审核报告中明确开出不符合项目要求该版本的要求针对于MDD指令和AIMD指令,全套CE技术文件编订,将要申请或者已经拿到了TUV莱茵、TUV南德、***或其他公告机构CE证书的企业,一定要高度关注。
CE技术文件编订
全套CE技术文件编订临床报告的内容:
1、器械的性能测试报告;
2、器械的依据协调标准进行的测试报告;
3、器械PMS数据;
4、器械的PMCF的数据;
5、文献资料中搜集到的器械*和性能的数据;
6、比对器械的数据。
CE技术文件编订
全套CE技术文件编订相对于之前的临床报告,第四版的临床报告主要变化体系在:
1.临床报告更新的频率
2.报告编写人和评价人的资质
3.评估报告需要有明确的可测量目标
4.确定技术发展水平
5.数据的科学性和有效性
6.比对器械
7.比对器械的数据获得
8.什么时候需要临床试验
9.售后监督和售后临床跟踪
10.风险—收益。

至2020年5月26日,MDR法规将*强制实施