- 2024-05-16 08:20 4512
- 产品价格:面议
- 发货地址:上海金山 包装说明:不限
- 产品数量:9999.00 个产品规格:不限
- 信息编号:261301984公司编号:14235332
- 袁小姐 经理 微信 13818104617
- 进入店铺 在线留言 QQ咨询 在线询价
洛阳MDRCE认证厂
- 相关产品:
产地:上海可售地:**品牌:SUNGO型号:SUNGO BV包装:纸质
医用防护服、隔离衣、手术衣产品在进入欧盟市场前,企业需根据产品的预期用途,结合欧盟器械法规(EU)2017/745中附录Ⅷ要求,将产品分为I类、II类及III类,产品风险等级越高,分类等级越高,进入欧盟市场要求越高。
医用防护服、隔离衣、手术衣在MDR中属于Ⅰ类产品,风险等级相对较低,对于非级医用防护服、隔离衣、手术衣和级医用防护服、隔离衣、手术衣,产品走的认证途径也不一样。
解读MDR系列讨论 部分:MDR演变过程和MDR的过渡期MDR演变过程近两年,国内外器械法规变化巨大,对于器械厂家及从业人员来说,都面临着比较大的挑战,针对明年将要实施的欧盟器械新法规2017/745/EU MDR,小编精心为大家准备了解读MDR系列,旨在为从业的朋友们提供有价值的参考信息。

关于欧盟CE 认证的MDR法规升级:
老指令MDD 93/42/EEC including 2007/47/EC 升级到新法规MDR EU 2017/745
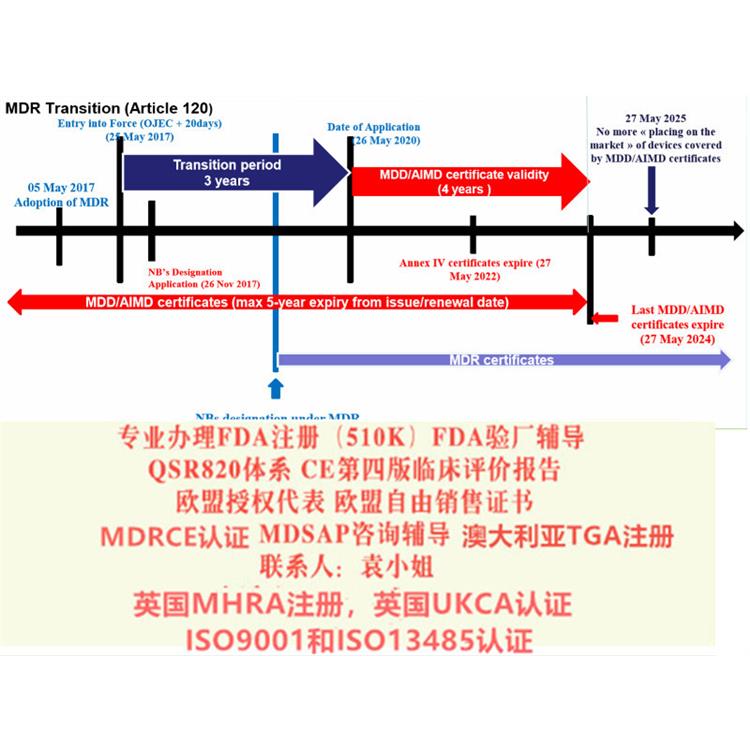
2017年5月,欧盟器械新法规MDR (REGULATION EU 2017/745) 颁布,新的法规将替代原有的器械指令 (MDD 93/42/EEC) 和有源植入性器械指令 (AIMDD 90/385/EEC) 。
从2020年5月开始公告机构不能按照MDD颁发CE证书,目前I*及以上风险等级产品认证机构已不再受理MDD指令的认证申请。
对于目前获得CE证书的企业,应基于自身设备的证据的充分性合理安排申请MDR的时间,尽快启动MDR法规合规准备事宜。

MDR于2017年5月发布,标志着MDD和AIMDD之间为期三年的过渡期的开始。在过渡期间,MDR将逐步生效,先是与公告机构和制造商根据MDR申请新证书的能力有关的规定。过渡期将于2020年5月26日,即MDR法规的“适用日期”(DoA)结束。从那时起,MDR将完全适用。
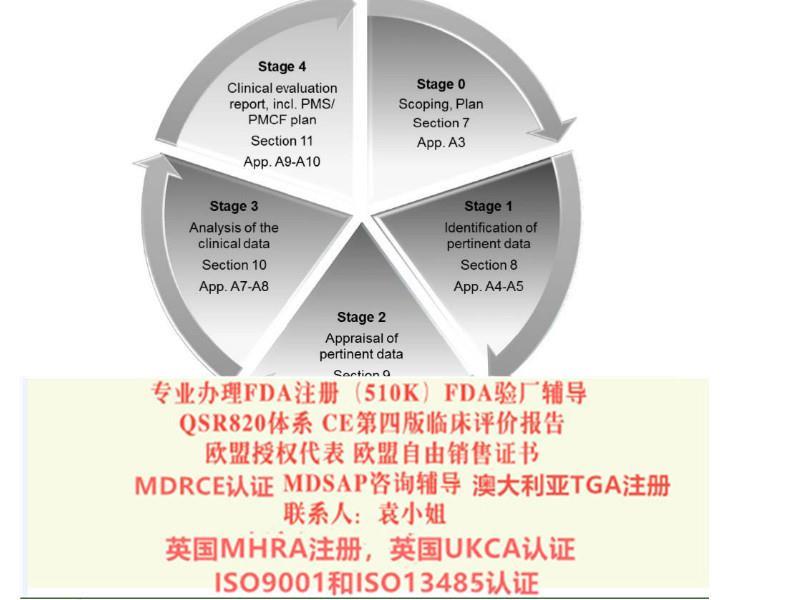
主要变化之五:数据的科学性和有效性
第四版评估指南非常强调数据的科学性和有效性,包括从统计学考虑。这贯穿于整个指南文件规定的阶段,包括影响数据完整性的因素,数据的客观性和权重,文件搜集的方法,数据的评估和权重,数据是否阐述了符合性的分析。
在此期间,仍然可以进行以下MDD的相关活动,例如产品变更及一年期内MDD新户的申请;现有MDD客户更新的相关活动;现有MDD客户更新的申请(包括提前更新的申请);现有MDD客户重大变更的申请期。虽然MDR的正式实施有延期,但是有例外情况如: · MDD产品的投放截止日期仍为2024年5月26日 · MDD产品供应截止日期仍为2025年5月26日。